Kompleksowe usługi dla przemysłu farmaceutycznego: chmura, walidacja i systemy jakości

Chmura farmaceutyczna
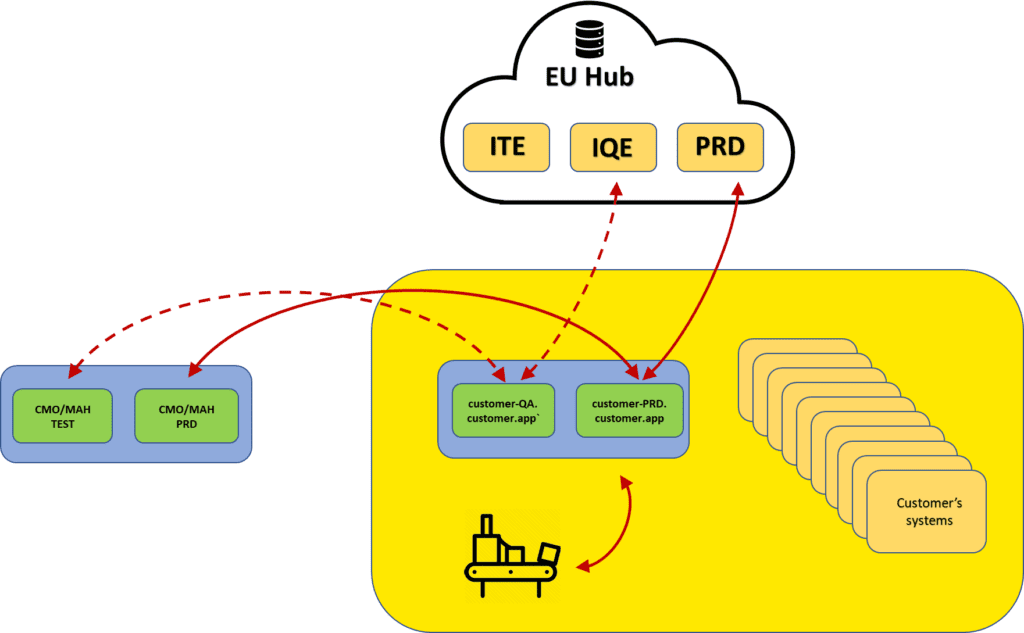
Chmura farmaceutyczna Introl Cloud jest dedykowaną przestrzenią sprzętową PaaS dla systemów skomputeryzowanych używanych w przemyśle. Rozwiązanie zapewnia outsourcing zadań działów IT i kwalifikacji w zakresie bezpieczeństwa i utrzymania infrastruktury. Stosowane zabezpieczenia oraz sposób wykonywania i przechowywania kopii zapasowych zapewniają zarówno bezpieczeństwo danych jak i spełniają wszelkie wymagania branżowe. Dodatkowe komponenty wdrożone w chmurze umożliwiają zewnętrzne integracje systemów zarówno z centralnymi i krajowymi repozytoriami danych jak i partnerami kontraktowymi.
Do głównych zalet Chmury farmaceutycznej można zaliczyć:
- zgodność z wymaganiami prawnymi,
- pewność ochrony i bezpieczeństwa danych,
- ograniczenie kosztów licencji i sprzętu IT,
- outsourcing usług IT.

Walidacja
Posiadamy własny zespół prowadzący prace kwalifikacyjne i walidacyjne dla realizowanych projektów oraz rewalidacje istniejących systemów. Ekspercka kadra posiada ponad 15-letnie doświadczenie pracy w środowisku EU GMP. Dostarczamy pełną dokumentację w języku polskim.
Ponadto w ramach prac kwalifikacyjnych i walidacyjnych, świadczymy usługi takie jak:
- walidacja czyszczenia,
- zanieczyszczenia krzyżowe,
- zarządzanie ryzykiem w jakości,
- przygotowanie zakładów do inspekcji,
- rozwiązywanie zgłaszanych problemów – analiza GAP,
- walidacja procesowa i optymalizacja procesów wytwarzania.

Konsulting
Weryfikujemy, analizujemy procesy, dane pod kątem spełniania wymagań prawnych oraz jakościowych kryteriów akceptacji. Weryfikujemy, analizujemy i sprawdzamy rozwiązania projektowe koncepcji pomieszczeń, instalacji HVAC oraz wytycznych dla automatyki HVAC, RMS, BMS pod kątem spełniania wymagań prawnych oraz jakościowych kryteriów akceptacji klienta. Podajemy rozwiązania optymalizujące procesy zgodnie z dostępną technologią. Wykonujemy analizę luk. Podajemy rozwiązania optymalizujące procesy zgodnie z dostępną technologią. Wskazujemy ryzyka i sposoby jego obniżania. Wspieramy osoby zarządzające procesami i właścicieli procesów prezentując stan zastany i niezbędne optymalne, odpowiedzialne działania do poprawy zgodności z wymaganiami EU GMP.
…dziś planujemy, jak będzie wyglądało jutro
- obiektywna ocena procesów wspiera trafność decyzji osób odpowiedzialnych,
- dostarczamy wyniki oceny i propozycje rozwiązań,
- pomagamy opracować i wdrożyć optymalne plany poprawy oraz rozwoju.

Outsourcing
Dostarczanie usług z zakresu Zapewnienia Jakości – zapewniamy wsparcie w walidacji procesowej, przygotowaniu do inspekcji, przeglądów okresowych, kwalifikacji/rekwalifikacji budynków, systemów skomputeryzowanych, systemów pomocniczych – HVAC, wody oczyszczonej, sprężonego powietrza i innych, systemów pomiarowych, przeglądów, kontroli zmian, CAPA, zarządzania ryzykiem, w tym zarządzania ryzykiem zanieczyszczeń krzyżowych, walidacji czyszczenia i innych.
Zapewniamy merytoryczne wsparcie i pomoc przy spiętrzeniu prac opracowując dokumentację. Posiadamy doświadczenie usprawnień i ułatwień w utrzymywaniu statusu zwalidowanego/skwalifikowanego produktów leczniczych i systemów wspierających. Optymalizujemy działania odpowiednio do wymagań EU GMP.
- Zarządzanie ryzykiem
- Konsulting, doradztwo i optymalizacja
- Walidacja/rewalidacja
- Audyty zewnętrzne i wsparcie przy inspekcji

Inspekcja a farmaceutyczny system jakości
Farmaceutyczny System Jakości jest podstawą działania firmy farmaceutycznej. Do jego doskonalenia i planowanie kierunków rozwoju wymagana jest jednak nie tylko specjalistyczna wiedza oraz doświadczenia, ale również obiektywizacja oceny poziomu wdrożenia i utrzymania.
- Wyznaczenie obszarów wytwarzania wymagającego przygotowania do
Inspekcji zgodnie z potrzebami klienta. - Ustalenie zakresu wymagań prawnych i norm wspierających spełnianie
wymagań (lista wytwarzanych produktów , prowadzonych procesów,
specjalnych warunków itp.). - Ustalenie dokumentacji odniesienia stanowiącej dowody spełniania wymagań
( procedur, instrukcji planów , protokołów , raportów i in). - Ustalenie bezpiecznego sposobu udostępniania dokumentacji.
- Opracowanie matrycy wymagań do odnotowania wyników audytu zdalnego:
– wprowadzenie danych,
– kwantyfikacja spełniania wymagań w %,
– wyznaczenie obszarów do doskonalenia - Propozycje działań CAPA pilnych i długofalowych strategii rozwoju.